近日,我院药学部研究员、副主任药师汤志远团队联合澳门科技大学等单位,在解析肝细胞癌仑伐替尼耐药发生发展的关键机制研究中取得重要进展,研究成果以“Lactylation Converts ABHD6 into a Mitochondrial Regulator that Drives Lenvatinib Resistance in Hepatocellular Carcinoma”为题,于3月20日在肿瘤学权威期刊《Cancer Research》在线发表(In-Press Preview)。该研究首次揭示了ABHD6在乳酸化修饰驱动下由经典代谢酶向线粒体调控因子转变,进而促进肝细胞癌对仑伐替尼产生耐药的分子机制。
肝细胞癌(hepatocellular carcinoma,HCC)是全球癌症相关死亡的主要原因之一,我国新发病例和死亡病例均占较高比例。仑伐替尼作为晚期肝癌一线靶向治疗药物,虽可改善部分患者生存获益,但约半数患者在治疗后6至7个月内会出现耐药,严重限制了临床疗效。长期以来,肝癌靶向治疗耐药的发生机制复杂,尤其是代谢重编程与线粒体适应性改变如何共同驱动耐药,始终是该领域亟待解决的重要科学问题。
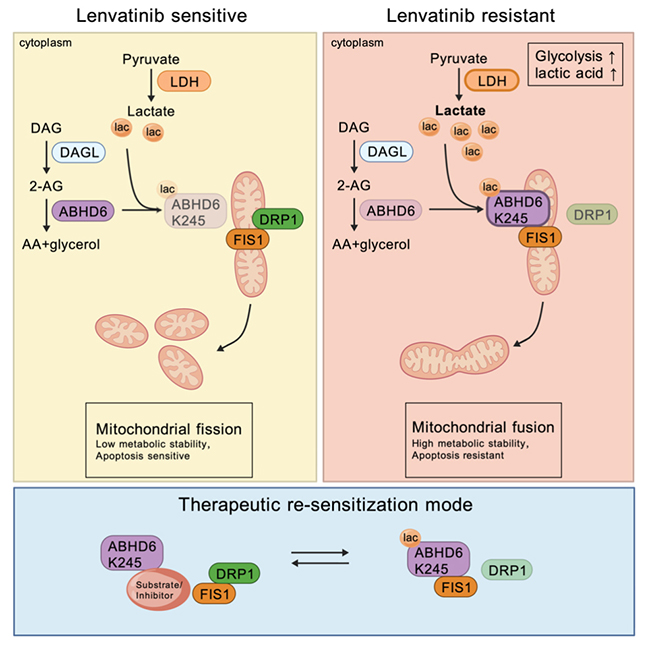
该研究从临床耐药问题出发,综合应用单细胞转录组分析、代谢组学、基因编辑、蛋白互作分析及动物模型等多种技术手段,鉴定出ABHD6是驱动肝癌仑伐替尼耐药的关键分子。研究发现,耐药肿瘤细胞中Warburg效应增强导致乳酸积累,诱导ABHD6发生K245位点乳酸化修饰,进而促进其转位至线粒体,并以非经典“支架蛋白”方式竞争性结合线粒体分裂调控蛋白FIS1、排斥DRP1,破坏线粒体分裂机制,稳定线粒体高融合状态,从而抑制药物诱导的活性氧生成和细胞凋亡,最终导致仑伐替尼耐药。进一步研究表明,ABHD6促耐药作用并不依赖其传统酶活性,而与其催化位点S148是否被占据密切相关;通过抑制乳酸生成或采用ABHD6特异性抑制剂占据其催化位点,可阻断ABHD6-FIS1复合物形成,恢复线粒体分裂并重新增强肿瘤细胞对仑伐替尼的敏感性。该研究提出了“乳酸化修饰―ABHD6构象/功能转换―线粒体动力学重塑―靶向治疗耐药”的全新机制链路,为肝癌精准治疗提供了新的理论依据和干预靶点。
此项工作由我院药学部牵头完成,汤志远、澳门科技大学朱依谆教授、丁倩教授为论文共同通讯作者,我院药学部孙悦宁博士、罗丞局博士及研究生杨慧和叶嘉欣为论文共同第一作者。研究得到国家自然科学基金,江苏省卫健委,南通市科技局等多项课题支持。
(供稿:科技处)